药物临床试验进入全过程监管时代,医疗机构、药企等该如何做
随着我国药物临床试验开展数量逐年递增,保证其过程规范性、数据可靠性等变得必要且迫切。
今年7月3日,国家药监局发布《药物临床试验机构监督检查办法(试行)(征求意见稿)》(下称《机构检查办法》),提出将研究机构、研究者同期承担临床试验项目较多等可能影响试验质量的问题纳入检查重点。7月10日,国家药监局药品审评中心发布《药品审评中心药物临床试验期间安全信息评估与风险管理工作程序(试行)修订稿(征求意见稿)》(下称《工作程序》),旨在进一步规范药物临床试验中的安全风险。
上述药物临床试验领域连续发文的要义何在?医疗机构、申办方(药企)和合同研究组织需要怎么做?
强调全过程监督管理
《中国新药注册临床试验进展年度报告(2021年)》相关数据显示,2021年,我国药物临床登记与信息公示平台登记临床试验总量已突破3000余项,较上一年增加29.1%;其中,新药临床试验数量为2033项,较上一年增加38.0%。
“新一轮的《药品管理法》修订,简化了药物临床试验机构办理流程,由许可改为备案管理;而为了进一步规范临床试验机构管理,则需加大日常检查的力度。”上海市食品药品安全研究会副会长兼秘书长魏俊璟告诉第一财经。
魏俊璟表示,《机构检查办法》以2019年12月发布的《药物临床试验机构管理规定》为基础,从国家层面对药品监督管理部门开展药物临床试验机构监督检查工作的职责、标准、程序和结果处理等进行了细化和完善,并统筹了地方制定的检查标准,明确了备案后首次检查、日常检查、有因检查、其他检查等类型,完善了药物临床试验监管体系的构建。
“《机构检查办法》和《工作程序》目前都是征求意见稿,还没有正式执行,都是对前期工作的一个延续。”中国医药质量管理协会临床试验合同研究组织分会副秘书长、博济医药首席运营官夏其奎表示。
夏其奎称,《机构检查办法》是对临床试验机构如何进行监管,强化临床试验机构在临床试验中的责任主体;《工作程序》则是对药审中心临床试验管理处在临床试验期间的安全风险评估管理的职责分工、沟通交流、工作时限做了细致说明,对相关工作程序进行规范。
“对于机构,此次文件强调了事中、事后层面更为规范化的监管方法,相信以后还会出来标准或者细则。而从药企角度来讲,选择怎样的机构来开展临床试验也很重要,可以纳入‘有因检查’中的三项内容作为判定依据。”夏其奎说。
作为临床试验机构方,中国医科大学某附属医院临床研究相关负责人告诉记者,原先,国家药监局对于机构的监督检查重点是“两头抓”,也就是最初进院时的审批准入和最终结项时的质量审核,“根据《机构检查办法》,将来会有更多对于药物临床试验整体过程的规范管理”。
如何兼具“速度”与“质量”
一项药物临床试验的开展如何兼具速度与质量?业内人士认为,速度与质量的提升由多种综合因素决定,还需注意维护好受试者的利益,保障好他们的生命安全。
“药物临床试验速度与质量的提升,一方面与临床试验方案最初设计有关,另一方面还与临床试验方案的具体执行有关。”魏俊璟表示,详细来说,机构应严格按照药物临床试验质量管理规范(GCP)来进行实操,合同研究组织则应更加关注GCP中的检查要求,以免因临床试验过程的合规问题导致临床试验失败,并使临床试验机构、主要研究者承担相应的法律责任。
而在夏其奎看来,团队、流程、能力缺一不可。在团队上,牵头单位、PI(主要研究者)的选择需要起到示范作用,同时,有高质量、有经验的合同研究组织加入才能共同形成一个能够打胜仗的临床试验研发团队;在流程上,绝大多数公司都拥有一套适用于自身的标准化体系,但于创新药而言,则更需要有针对药物临床试验的可灵活进行剪裁与适配的标准流程,该流程敏捷、自洽且整体遵循行业法规;在能力上,医学、注册、临床运营各方面的能力需要考虑,否则事倍功半。
夏其奎还提醒说,在进一步维护和保障受试者的利益和安全层面,药企一方面要进一步完善公司管理体系,包含运营体系和药物警戒体系等;另一方面,在实际运营临床试验的过程中,要把保护患者利益放在第一位,不断去培训团队人员。
此外,数字化、智能化工具也是提升药物临床试验速度和质量,并帮助受试者避免安全风险的关键。
上述医院临床试验研究负责人表示,机构可以建立覆盖数据录入、伦理审查、质量控制等环节的全过程信息管理系统,“这样一来,相关信息调动较为方便,一旦发生了违背方案或者操作不合理、不合规等情况,系统就可以立即提示和预警,从而全面提升临床试验的速度和质量。往常,药物临床试验通过纸质版记录,再经过几周时间上报,有些滞后。将来,机构、药企、合同研究组织三方可以更直观地了解到药物临床试验的进展。”
更多项目正在下沉
药物临床试验数量递增,尽管为释放临床资源、缓解供需矛盾、满足临床试验需求等提供了有效解决方案,但仍有一些亟待完善的缺陷。
夏其奎告诉记者,目前,我国药物临床试验的项目主要落地在一些一二线城市的三甲医院,覆盖受试者的数量并不特别充分;同时,药物临床试验机构数量增长速度快,但项目的分配并不是很均匀,有科室每年承接了过多同质化项目;此外,CRC(临床试验协调员)、CRA(临床试验监查员)、PI的职责在实际运营时不太清晰,这需要通过多方努力来进一步明确。
数据显示,2022年所有全国临床试验机构类型中,由于综合条件和资源等优势,三级医院依然是药物临床试验机构的主体。三级医院共有463家,占比39.04%,二级医院和其他机构分别为46家和41家,血液中心仅有1家。
为此,上述医院临床试验研究负责人建议,三甲医院可以和辖区内拿到GCP资质的二级医院、县级医院等形成区域临床研究中心,在制定相关协同标准(包括伦理互认)的基础上,将一些同质化的药物临床试验项目分配出去;当然,在制定相关协同标准时,需要纳入合规、合理的工作要求和程序,并对PI进行必要培训。
该负责人表示,二级医院、县级医院其实在糖尿病、心脑血管等慢病管理方面有很强的优势,并且存在一定的患者基数,应鼓励这些机构参与药物临床试验,这有助于提高基层医生的诊疗规范和研究水平。
“二级医院、县级医院可能暂时不具备牵头疑难药物临床试验的基础,其对于相关受试者的安全风险、数据质量控制等能力也较弱,一些慢性疾病会是比较好的项目选择。与此同时,一些平台在二级医院、县级医院进行受试者招募的过程中,也需要加强健康科普教育,减少患者顾虑。”该负责人补充说。
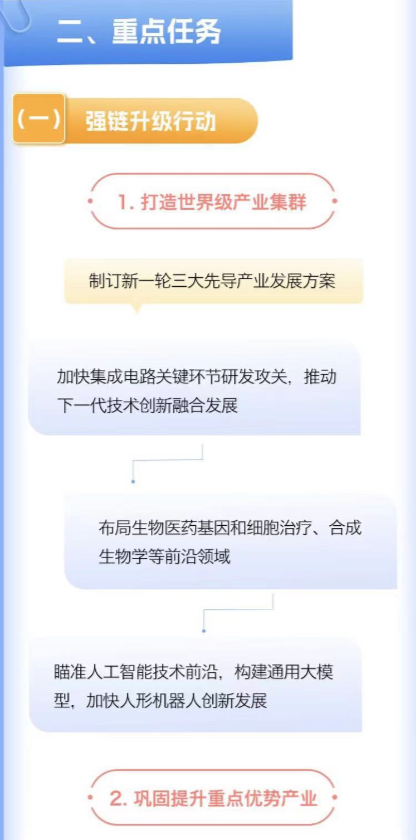
4个万亿产业集群、新一轮三大产业方案,上海制造业未来怎么干
行动计划实施6大行动、22项重点任务把制造业作为实体经济主战场的上海,正加快构建新型产业体系,打造高端制造业增长极。6月15日,上海市公布了《上海市推动制造业高质量发展三年行动计划(2023-2025年)》(下称“行动计划”),提出到2025年,“2(36)(45)”现代化产业体系不断夯实,工业增加值超过1.3万亿元,占地区生产总值比重达25%以上,工业投资年均增长5%。锤子财富2023-06-15 17:27:590000增量扩面 优化结构 新金融推动普惠金融高质量发展
未来,建行将持续大力推进金融服务实体经济,坚持系统观念、守正创新。小微企业是促进发展、稳定就业、保障民生的重要依托,是提升产业链供应链稳定性和竞争力的关键环节,是构建新发展格局的有力支撑。0002东南亚市场“造车热”,smart与宝腾汽车探讨海外建厂可行性
如今借助宝腾汽车这个“据点”,吉利系正在大举进入东南亚市场。东南亚正在成为中国车企出海热门地。近日,smart与宝腾汽车正式签署深化合作备忘录。双方将结合资源优势,全方位深化合作,包括但不限于探讨“构建海外生产能力”的可行性。与此同时,smart精灵#1马来西亚右舵版也在当地开启预售,并将按计划在今年第四季度正式交付。锤子财富2023-09-25 21:50:340000分别提高1000元!国务院调整三项个税专项附加扣除标准
3岁以下婴幼儿照护专项附加扣除标准,由每个婴幼儿每月1000元提高到2000元。子女教育专项附加扣除标准,由每个子女每月1000元提高到2000元。赡养老人专项附加扣除标准,由每月2000元提高到3000元。为进一步减轻家庭生育养育和赡养老人的支出负担,依据《中华人民共和国个人所得税法》有关规定,国务院决定,提高3岁以下婴幼儿照护等三项个人所得税专项附加扣除标准。0000中东两大主权基金持有61只A股,偏爱工业制造细分龙头
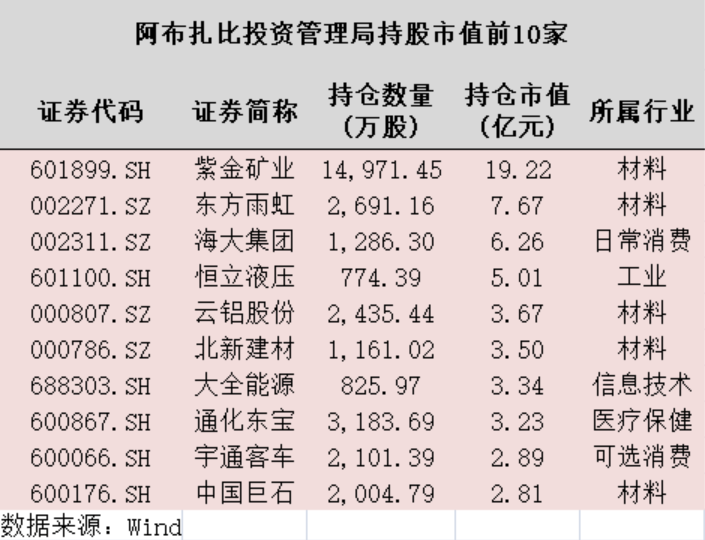
两家主权基金持股几乎没有重叠,唯一共同持有的个股是恒立液压。“不差钱”的中东土豪,二季度大手笔买入了生物医药、有色金属等行业,或是继续坚定持有先前布局的一些细分赛道龙头股,令市场对相关板块及个股后期行情的期待有所升温。锤子财富2023-09-13 22:42:420000